Baca berita dengan sedikit iklan, klik di sini
Ringkasan Berita
Hampir dua lusin perusahaan bioteknologi di dunia berlomba mengembangkan vaksin untuk virus SARS-Cov-2.
Perusahaan pembuat vaksin Moderna Inc dari Cambridge, Amerika Serikat, menjadi yang pertama melakukan uji klinis fase I untuk vaksin bernama mRNA-1273 pada 16 Maret lalu.
Meskipun uji klinis sukses, mustahil dapat menyediakan vaksin Covid-19 di pasar dalam waktu setahun ke depan.
JENNIFER Haller, 43 tahun, ibu dua anak dari Seattle, Amerika Serikat, sangat percaya diri saat lengan kirinya ditembus jarum suntik di markas Kaiser Permanente Washington Health Research Institute, Senin, 16 Maret lalu. Pekerja perusahaan teknologi itu menjadi relawan pertama dari 45 orang yang ikut uji klinis fase pertama vaksin untuk virus SARS-Cov-2 yang bernama mRNA-1273. “Tak ada risiko bagi saya terpapar virus itu,” ujar Haller dengan yakin kepada CNN.
Baca berita dengan sedikit iklan, klik di sini
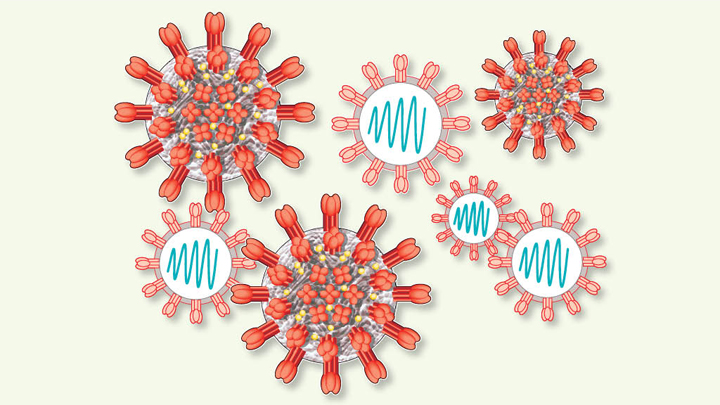
Bakal vaksin bikinan National Institute of Health (NIH) bersama perusahaan bioteknologi Moderna Inc itu memang tak mengandung virus hidup yang dilemahkan. Sebagai gantinya adalah molekul asam ribonukleat (RNA) virus sintetis. Tipe RNA-nya adalah RNA kurir (mRNA) yang mengandung instruksi ke sel-sel virus untuk menciptakan protein spike—yang berbentuk paku mahkota. Protein spike inilah yang menempel di dinding sel inang dan menginfeksinya.
Baca berita dengan sedikit iklan, klik di sini
Baca berita dengan sedikit iklan, klik di sini

Peneliti berharap dengan menyuntikkan mRNA virus ke tubuh manusia akan memperoleh respons imun yang kuat. Bila protein asing itu terdeteksi, sistem kekebalan tubuh akan membuat antibodi untuk menyerangnya dan lebih siap bereaksi bila virus Covid-19 alami kelak menyerang. “Kami tak tahu apakah vaksin ini menyebabkan respons imun. Itulah perlunya uji klinis,” kata kepala pengujian Lisa Jackson dari Kaiser Permanente.
Memakai mRNA sintetis merupakan cara cepat memproduksi vaksin ketimbang metode tradisional yang harus menumbuhkan virus hidup di laboratorium. Moderna hanya butuh 42 hari mengembangkan bibit vaksin sejak 13 Januari lalu hingga mengirimnya ke NIH pada 24 Februari lalu. Hal itu berkat Yong-Zhen Zhang dari Fudan University, Shanghai, Cina, dan tim yang berhasil mengurutkan gen virus SARS-Cov-2 dan membagikannya di Virological.org pada 11 Januari lalu.
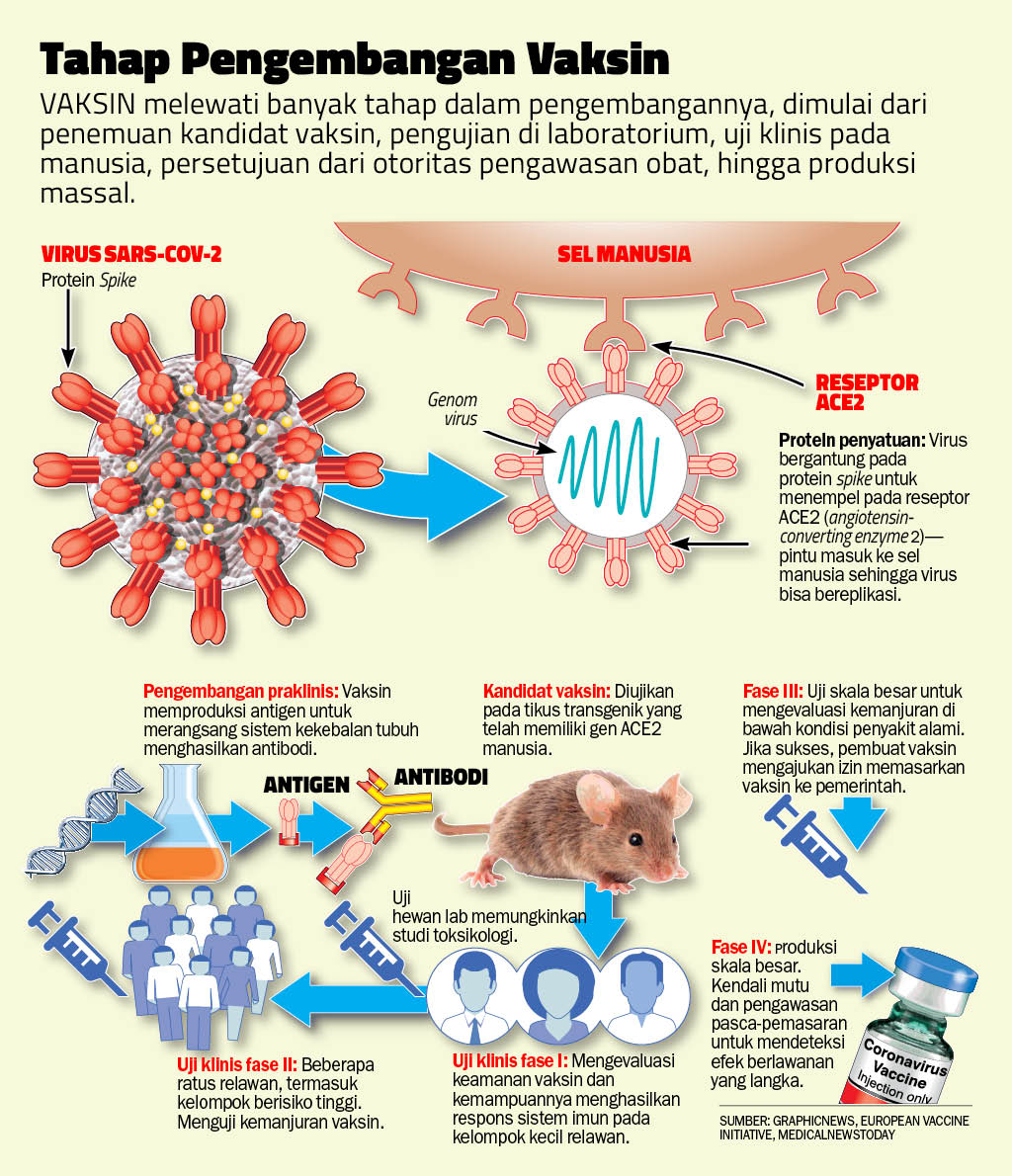
Menurut Anthony S. Fauci, Direktur National Institute of Allergy and Infectious Diseases NIH, walaupun uji klinis berjalan mulus, vaksin itu mustahil tersedia di pasar dalam 12-18 bulan ke depan. Ada banyak tahap pengembangan vaksin. Tahap akhir biasanya menjadi leher botol karena pendaftaran dan persetujuan otoritas serta produksi massal bisa membutuhkan waktu hingga satu dekade. “Vaksin tetap penting jika virus jadi ancaman jangka panjang,” ucap Fauci.
Vaksin ebola menjadi contoh betapa lama pengembangan vaksin. Ebola terdeteksi oleh para saintis pada 1976. Tapi, hingga wabah itu menghantam Afrika Barat pada 2014, tak satu pun vaksin yang dikembangkan. Bibit vaksin rVSV-ZEBOV yang dikembangkan Merck baru diuji-kliniskan di Guinea ketika wabah itu menginfeksi 28 ribu orang pada 2016. Vaksin itu mendapat sertifikasi Badan Kesehatan Dunia (WHO) pada November 2019 serta persetujuan Badan Pengawas Obat dan Makanan Amerika (FDA) sebulan kemudian.
Coalition for Epidemic Preparedness Innovations (CEPI) mungkin tidak merujuk pada pengalaman vaksin ebola itu. Koalisi global yang bermarkas di Oslo, Norwegia, itu bertekad memiliki vaksin Covid-19 dalam waktu enam bulan. CEPI, yang didirikan pemerintah Norwegia dan India, Bill & Melinda Gates Foundation, Wellcome Trust, serta World Economic Forum, telah mensponsori delapan konsorsium pengembang vaksin, termasuk proyek mRNA-1273.
Inovio Pharmaceuticals Inc juga mendapat dukungan dana US$ 9 juta dari CEPI untuk membuat vaksin asam deoksiribonukleat (DNA) bernama INO-4800. Inovio, yang bermarkas di San Diego, California, Amerika, mengklaim telah mendapatkan bibit vaksin itu tiga jam setelah urutan gen virus SARS-Cov-2 dipublikasikan. Pembuatannya via teknik pemetaan digital urutan DNA virus, yang juga sukses membuat vaksin sindrom pernapasan Timur Tengah (MERS) yang telah diuji klinis fase II.
Ada hampir dua lusin perusahaan bioteknologi, sebagian besar asal Amerika, berlomba menciptakan vaksin Covid-19. Di antaranya Novavax Inc, Heat Biologics Inc, Janssen Pharmaceutical Companies Johnson & Johnson, Sanofi, dan Vaxart Inc. Perusahaan-perusahaan tersebut ada yang mendapat pendanaan dari Biomedical Advanced Research and Development Authority (BARDA) Departemen Kesehatan Amerika dan NIH. Ada pula yang didanai CEPI.
Di daratan Eropa, ada BioNTech SE dari Mainz, Jerman, yang mengembangkan vaksin mRNA bernama BNT162. Vaksin itu akan diuji-kliniskan pada akhir April nanti, menggandeng Shanghai Fosun Pharmaceutical Group. Perusahaan Jerman lain, CureVac AG, yang berbasis di Tübingen juga mengembangkan vaksin mRNA. Selain itu, Institut Pasteur Prancis menggandeng Themis Bioscience dari Austria mengembangkan vaksin berdasarkan teknologi vaksin campak.
Di Australia, University of Queensland di Brisbane mendapat dukungan CEPI dan Commonwealth Scientific and Industrial Research Organisation (CSIRO) mengembangkan vaksin dari protein spike virus yang mereka juluki vaksin molecular clamp. Sementara itu, di Israel, MIGAL Galilee Research Institute Ltd tak mau ketinggalan mengembangkan vaksin Covid-19 yang berbasis teknologi vaksin Infectious Bronchitis Virus, yang menyerang ternak unggas.
Perusahaan Cina, CanSino Biologics, juga tak mau kalah dari Moderna dalam menggelar uji klinis fase I. Perusahaan yang bermarkas di Tianjin itu bekerja sama dengan Institute of Biotechnology pada Academy of Military Medical Sciences menguji klinis vaksin yang dinamai Ad5-nCoV kepada 108 relawan. Ad5-nCoV adalah kandidat vaksin rekayasa genetika dengan bagian replikasi adenovirus tipe 5 sebagai vektor untuk mengekspresikan protein spike virus.
Indonesia juga hendak mengembangkan vaksin Covid-19 sendiri. Menurut Amin Soebandrio, Direktur Lembaga Biologi Molekuler Eijkman, Jakarta, pihaknya ditunjuk oleh Menteri Riset dan Teknologi untuk memimpin konsorsium pengembangan vaksin. “Ditargetkan dalam waktu 12-18 bulan sudah ada bibit vaksin yang siap diserahkan ke industri, dalam hal ini PT Bio Farma, untuk diproduksi,” tutur Amin kepada Tempo, Rabu, 18 Maret lalu.
Lembaga Eijkman, kata Amin, berpengalaman membuat vaksin flu burung untuk unggas. “Kami bisa membuat bibit vaksin dalam waktu 10 bulan pada 2011,” ujarnya. Amin menjelaskan dua strategi yang disiapkan dalam membuat vaksin untuk manusia, yakni mempelajari antigen yang bisa dipakai untuk vaksin dan menggunakan informasi genetik virus yang ada di GenBank untuk membuat peptidanya secara sintetis sebagai bahan vaksin.
DODY HIDAYAT, GABRIEL WAHYU TITYOGA (WIRED, TIME, REUTERS, CEPI, MARKETWATCH)
- Akses edisi mingguan dari Tahun 1971
- Akses penuh seluruh artikel Tempo+
- Baca dengan lebih sedikit gangguan iklan
- Fitur baca cepat di edisi Mingguan
- Anda Mendukung Independensi Jurnalisme Tempo